Teori struktur atom dalam ilmu fisika dan kimia mengarah pada sifat alamiah materi yang tersusun dari unit terkecil bernama atom. Ada berbagai macam teori tentang atom sampai akhirnya saat ini menggunakan model atom mekanika kuantum.
Setidaknya, teori atom yang dipakai saat ini tidak semerta-merta ada. Melainkan melalui proses teori yang cukup panjang seiring berjalannya waktu dan berkembangnya ilmu pengetahuan. Dengan mempelajari teori tentang atom, maka sifat kimia dan fisika suatu benda bisa diketahui.
Perkembangan Teori Struktur Atom
Teori tentang atom sudah ada sejak ribuan tahun lalu sehingga penting untuk dipelajari. Terutama bagi yang berkutat dengan ilmu fisika dan kimia, atom sendiri merupakan unit terkecil dari wujud benda. Lalu, apa saja teori mengenai atom dan tokoh yang mengemukakannya? Berikut ulasannya.
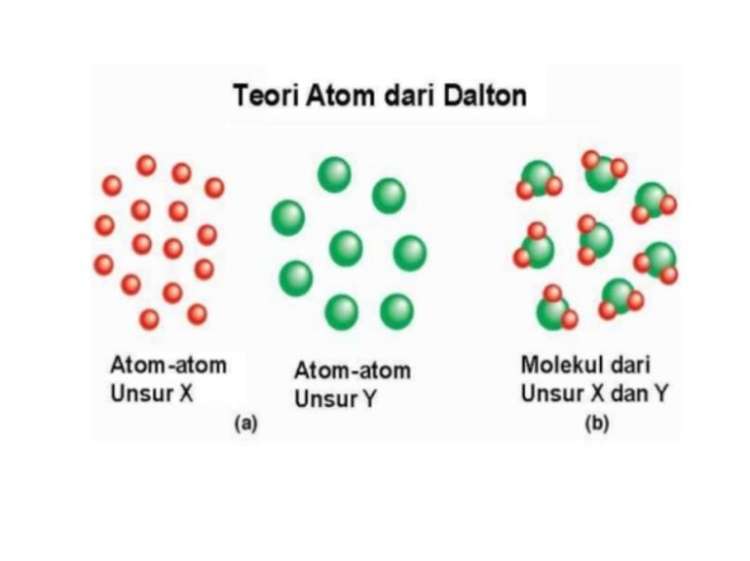
1. Teori Atom Dalton (1803)
Bisa dibilang, John Dalton merupakan tokoh pertama yang memulai teori mengenai atom, tepatnya di tahun 1803. Pada dasarnya, Dalton mengemukakan pendapatnya berdasarkan hukum kekekalan massa (Lavoisier) dan hukum susunan tetap (Proust).
Adapun beberapa point penting tentang teori model atom Dalton yang dikemukakan John Dalton adalah sebagai berikut.
- Atom merupakan unsur terkecil dari benda dan tidak dapat dibagi menjadi unsur lain lagi.
- Atom yang sejenis memiliki sifat sama.
- Terjadi penggabungan atau pemisahan unsur atom apabila dipancing dengan reaksi kimia.
- Atom bisa bereaksi dan bergabung dengan atom lainnya lalu membentuk molekul.
Sebagai pencetus teori struktur atom, teori yang dikemukakan dalton sayangnya memiliki beberapa kekurangan. Teori tersebut tidak menggambarkan bagaimana cara atom bereaksi dan bergabung membentuk molekul.
Selain itu, suatu jenis atom dengan atom lainnya tidak bisa dideskripsikan, begitu pula dengan sifat listrik materi. Tak heran jika pada akhirnya teori atom Dalton hanya bertahan selama 90 tahun. Terlebih hubungan antara daya hantar arus listrik dan larutan senyawa tidak dijelaskan.
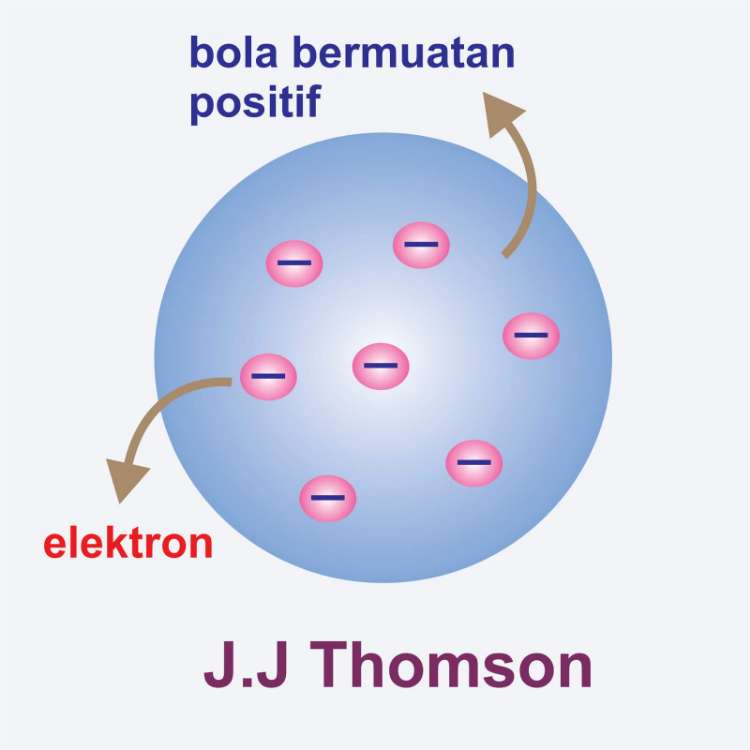
2. Teori Atom Thomson (1897)
Teori mengenai atom berikutnya adalah dari Sir Joseph John Thomson. Pada dasarnya, teori ini lahir setelah John Dalton mengemukakan pemikirannya mengenai atom. Adapun teori yang lahir tahun 1897 ini sebenarnya memperbaiki kekurangan-kekurangan yang ada.
Thomson saat itu menemukan partikel dalam materi yang memiliki muatan negatif, bagian tersebut selanjutnya disebut elektron. Pada dasarnya, elektron menjadi penemuan penting guna memperbaiki kekurangan yang ada pada teori di masa sebelumnya.
Beberapa inti dari teori model atom Thomson adalah sebagai berikut.
- Atom bukan unit terkecil dari suatu zat atau materi.
- Massa elektron kenyataannya lebih kecil jika dibandingkan massa atom keseluruhan.
- Atom bersifat netral karena muatannya ada yang positif dan negatif.
- Suatu atom tidak memiliki muatan positif dan negatif yang tidak seimbang atau berlebihan.
- Atom bermuatan positif tersebar merata ke seluruh bagian atom kemudian dinetralkan oleh muatan negatif.
Tidak jauh berbeda dengan teori atom Dalton, teori ini juga memiliki beberapa point kekurangan. Bagaimana tidak, teori atom satu ini sebenarnya tidak menjelaskan bagaimana susunan muatan atom terjadi.
Mengingat dalam teorinya, Thomson mengemukakan muatan positif dan elektron di dalam atom. Tidak hanya itu, inti atom juga tidak dapat dijelaskan dan teori ini tidak dikembangkan kembali.
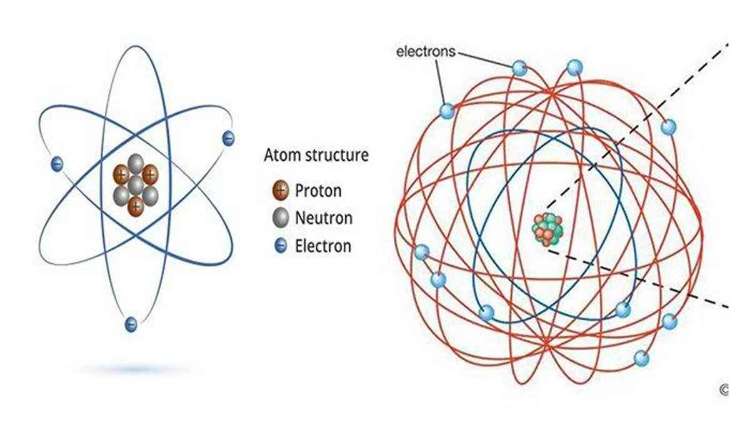
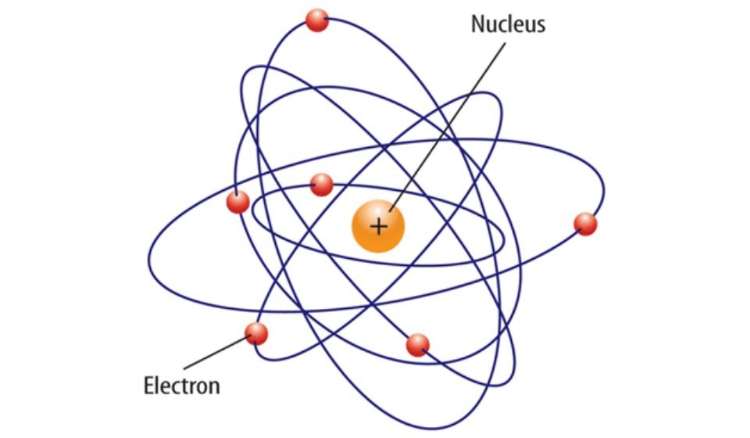
3. Teori Atom Rutherford (1910)
Teori model atom Rutherford ini dikemukakan oleh Ernest Rutherford yang berasal dari New Zealand. Meski demikian, ia berkewarganegaraan Inggris dan menjadi partner Thomson. Rutherford adalah murid Thomson yang kemudian mengembangkan dan memperbaiki teori atom gurunya tersebut.
Pada tahun 1910, Rutherford dan asistennya mengemukakan tentang inti atom. Pada dasarnya, inti bagian atom terdiri dari jari-jari yang lebih kecil dibanding jari-jari atom itu sendiri. Teori seperti ini berasal dari penelitian penembakan inti atom terhadap lempengan emas.
Berdasarkan penelitiannya, Rutherford berkesimpulan bahwa inti atom yang terkena partikel alfa akan membuat partikel tersebut memantul atau membelok. Hal ini karena adanya muatan atom dan massa yang berpusat pada inti. Adapun beberapa point penting mengenai teori ini adalah sebagai berikut.
- Atom terdiri atas inti atom yang memiliki muatan positif dan elektron yang bersifat negatif.
- Atom bersifat netral karena jumlah muatannya sama antara positif dan negatif.
- Ketika mengitari inti, terjadi gaya sentripetal pada elektron hingga terbentuk gaya lain. Gaya tersebut adalah gaya Coulomb yang terjadi antara elektron dan inti atom.
- Sebagian besar volume atom merupakan ruang kosong karena jari-jari inti lebih kecil dari jari-jari atom itu sendiri.
Sayangnya, teori struktur atom Rutherford ini tidak menjelaskan lebih rinci tentang cara rotasi inti atom. Begitu pula dengan letak elektron di dalamnya. Teori ini juga membuat energi atom menjadi tidak terlalu stabil karena memancarkan energi.
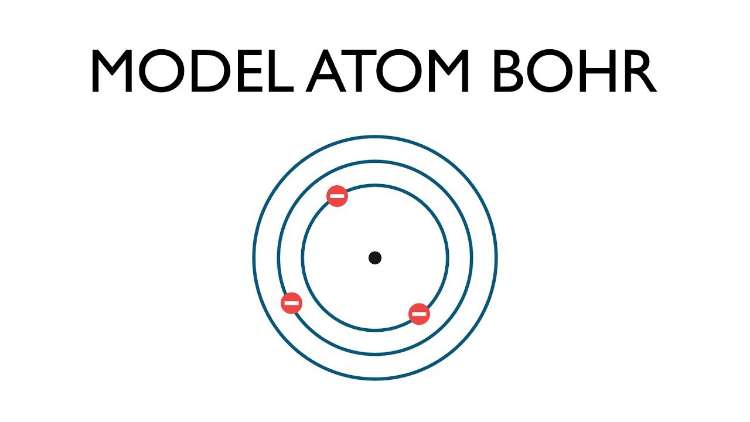
4. Teori Atom Bohr (1913)
Niels Bohr adalah seorang fisikawan berkewarganegaraan Denmark yang juga pernah mengemukakan teori atom. Peraih Nobel Fisika tahun 1922 ini memulai penelitiannya tentang atom di tahun 1913.
Pada saat itu, ia sudah memberi nama hasil penelitiannya dengan spektrum atom hidrogen. Bohr mengungkapkan bahwa teori atom layaknya peredaran planet saat mengitari tata surya.
Eksperimen yang dilakukannya menghasilkan pernyataan bahwa elektron-elektron yang mengelilingi inti atom terdiri dari dua bagian. Keduanya merupakan proton dan neutron yang melalui lintasan-lintasan tertentu dengan tingkat energi atau dikenal dengan kulit elektron.
Beberapa peneliti menyebut teori struktur atom ini sebagai Teori Atom Rutherford-Bohr karena secara tidak langsung merupakan modifikasi teori sebelumnya.Terdapat beberapa inti dari atom Bohr, yaitu sebagai berikut.
- Bagian elektron mengelilingi atom pada orbit tertentu.
- Selama berada di lintasan, energi elektron bersifat tetap sehingga tidak ada energi yang diserap maupun dipancarkan.
- Elektron hanya bisa berpindah dari satu tingkatan energi ke tingkatan lainnya dengan cara menyerap atau memancarkan energi.
Meski demikian, terdapat sejumlah kelemahan dari teori ini, yaitu tidak dapat menerangkan spektrum atom yang lebih besar dibanding hidrogen. Selain itu, teori atom ini tidak menjelaskan tentang efek Zeemon.
5. Teori Atom Mekanika Kuantum (1925)
Teori mekanika kuantum ini lahir guna menyempurnakan teori atom oleh Bohr. Teori satu ini pada awalnya dikemukakan oleh Erwin Schrodinger yang merupakan peraih Nobel Fisika tahun 1933 asal Austria.
Pendapat ini dikembangkan secara modern menurut hasil hipotesis de Broglie yang menyebutkan bahwa elektron memiliki dualisme sifat. Pertama, elektron bukan hanya sebagai partikel, melainkan gelombang yang memiliki lintasan.
Pada dasarnya, tidak hanya Schrodinger yang mengemukakkan teori struktur atom modern. Melainkan peneliti lainnya yang bekerja sama dengannya yaitu, Heisenberg. Pada akhirnya, kedua peneliti tersebut mengembangkan teori bernama teori atom mekanika kuantum.
Seperti yang telah diketahui, penelitian Schrodinger berdasarkan hipotesis de Broglie. Sementara itu, Heisenberg mengemukakan pemikirannya berdasarkan prinsip ketidakpastian Werner Heisenberg.
Kedua pemikiran tersebut menyimpulkan teori bahwa terdapat suatu keterbatasan untuk menentukan posisi pasti dari elektron. Dengan kata lain, teori mekanika kuantum disebut sebagai teori paling modern dan mutakhir dibanding teori lainnya yang sejenis.
Beberapa teori struktur atom yang disebutkan di atas pada dasarnya berkembang satu per satu. Dimulai dari teori atom John Dalton yang dikemukakan sekitar tahun 1803. Tahun tersebut merupakan awal mulanya teori ini berkembang sehingga akhirnya menjadi teori mekanika kuantum.